
2.10 Problematiche relative alla regolamentazione e alla gestione
Le problematiche che i mari del Regno Unito devono affrontare, descritte nel presente rapporto, sottolineano l’importanza di disporre di solide misure di tutela ambientale e di normative adeguatamente applicate. Il Regno Unito dispone di un buon quadro normativo in materia di protezione ambientale, che dovrebbe garantire che i nuovi progetti non abbiano un impatto negativo sulle specie e sugli habitat marini. Tuttavia, l'analisi condotta per il presente rapporto sull'ultimo Offshore Energy Strategic Environmental Assessment 217 (una valutazione volta a stabilire se gli impatti ambientali dei piani governativi in materia di energia offshore superino i benefici), ha evidenziato una vasta gamma di carenze relative alle normative sul petrolio e sul gas offshore.
Ciò indica che le normative ambientali non offrono necessariamente la protezione che dovrebbero.
Esistono prove evidenti che le compagnie petrolifere e del gas stiano conducendo valutazioni di impatto ambientale (VIA) di scarsa qualità nel valutare i progetti del petrolio e del gas offshore. 219 Le valutazioni di impatto ambientale dovrebbero segnalare i rischi ambientali e garantire che non vi siano effetti negativi sulle aree marine protette (AMP) o sull'ambiente in generale 218, tuttavia mancano valutazioni di impatto ambientale di alta qualità con misure di mitigazione degli impatti diretti significative ed efficacemente attuate 220.
Esistono prove evidenti che le società petrolifere e del gas
stiano conducendo valutazioni di impatto ambientale (VIA)
di scarsa qualità nel valutare i progetti
di sfruttamento offshore di petrolio e gas.
Una recente analisi ha raccomandato di migliorare il livello di dettaglio fornito nelle dichiarazioni ambientali in materia di inquinamento, rifiuti ed emissioni di gas serra, nonché di integrare metodi di mitigazione più efficaci e di standard più elevati. È stata inoltre sottolineata la necessità di un approccio più coerente nella valutazione degli impatti cumulativi, alla luce del numero crescente di progetti e delle crescenti minacce alla nostra fauna marina. Anche a livello internazionale sono state evidenziate le particolari problematiche legate alla realizzazione di VIA efficaci in ambienti di acque profonde,221 il che aumenta il rischio di un impatto maggiore derivante dagli sviluppi petroliferi (un buon esempio di ciò sono le sfide della modellizzazione delle fuoriuscite di petrolio per i siti profondi).37
Le carenze del processo di VIA sono evidenti nella valutazione della dichiarazione ambientale relativa allo sviluppo del giacimento Alligin da parte della BP, che si trova all’interno dell’Area Marina Protetta della Faroe-Shetland Sponge Belt. Si prevedeva che comportasse la perforazione di pozzi, una significativa infrastruttura sul fondale marino e lo scarico in mare di oltre 1500 tonnellate di fango a base acquosa e detriti di perforazione. Tuttavia, la BP ha affermato che il progetto non avrebbe avuto alcun impatto negativo significativo sull’area marina protetta (MPA). Si tratta di una zona nota per ospitare comunità di spugne di acque profonde, un habitat di interesse conservazionistico riconosciuto a livello internazionale 222, aggregazioni di vongole oceaniche e numerose specie di delfini e balene. La dichiarazione ambientale concludeva affermando: «Non si prevedono impatti negativi significativi tali da giustificare misure di mitigazione specifiche o condizioni di monitoraggio». Senza un esame critico, l’autorità di regolamentazione del Regno Unito ha acconsentito e approvato il progetto 223, che ha avviato la produzione nel febbraio 2020 224.

L’analisi ambientale che sta alla base di gran parte dell’approvazione e del processo decisionale relativo agli sviluppi energetici offshore si basa sul processo di Valutazione Ambientale Strategica (VAS) 225. Dall’analisi condotta per questo rapporto e dai feedback delle organizzazioni ambientaliste è emersa una tendenza generale di queste valutazioni a ignorare o minimizzare alcuni impatti degli sviluppi sull’ambiente marino. Inoltre, si verificano frequenti ritardi nell’inclusione di nuove prove o informazioni tecniche nelle risposte alle consultazioni, che spesso non vengono affatto adeguatamente prese in considerazione.
Nell'ultima valutazione, l'Offshore Energy Strategic Assessment 4 (OESEA4) 217, gli impatti dei rumori sismici sul comportamento dei mammiferi marini sono stati classificati come minori in quanto si tratta di «impatti a breve termine», nonostante le indagini richiedano spesso mesi per essere completate. Anche gli impatti delle trivellazioni sulla vita marina vengono minimizzati, nonostante una grande quantità di studi dimostri il contrario 60,71,74,226–228. Il rapporto governativo ha inoltre liquidato la questione degli scarichi contaminati delle trivellazioni, poiché si ritiene che si disperdano ampiamente e non si accumulino in quantità significative, nonostante le prove che gli IPA (idrocarburi policiclici aromatici) trovati nei cumuli di detriti di perforazione abbiano avuto effetti negativi dimostrabili sui pesci, tra cui emorragie e lesioni 229,230.
2.11 Buone pratiche internazionali
Alcuni paesi stanno adottando misure significative e aprendo la strada alla graduale eliminazione delle attività petrolifere e del gas offshore. Danimarca, Irlanda, Francia, Spagna, Belize, Groenlandia, Costa Rica, Svezia e Galles hanno tutti aderito alla Beyond Oil and Gas Alliance, lanciata alla COP26 a Glasgow nel 2021, e hanno tutti cessato il rilascio di nuove licenze e fissato obiettivi chiari per l’eliminazione graduale della produzione di petrolio e gas 234. Il Belize e la Groenlandia citano la protezione dell’ambiente marino come principale motore del cambiamento 235. L'approccio adottato da questi paesi tiene conto del fabbisogno attuale di petrolio e gas, in attesa che le alternative rinnovabili diventino la norma, e rispetta gli impegni di transizione equa aiutando le imprese e i cittadini a prepararsi e a pianificare i cambiamenti futuri. Alcune regioni e stati hanno adottato misure simili, tra cui il Nuovo Galles del Sud in Australia, che ha vietato l'esplorazione di petrolio e gas offshore nel 2022 236. Molti paesi hanno politiche specifiche relative alla protezione delle aree marine protette (AMP) dagli impatti del petrolio e del gas offshore. Nel 2019, il Canada ha vietato lo sfruttamento di petrolio e gas in tutte le sue aree protette 237, dopo aver deciso di adottare gli standard più elevati stabiliti nelle Linee guida dell’Unione Internazionale per la Conservazione della Natura (IUCN) 141,142, 238. Secondo quanto riferito, questa decisione è stata in parte una risposta alle proteste dell’opinione pubblica suscitate dall’annuncio che l’area marina protetta (AMP) del Canale Laurentiano – che tutela, tra l’altro, le zone di riproduzione dello squalo smeriglio, le tartarughe liuto e le penne di mare 239 – avrebbe consentito l’estrazione di petrolio e gas in tutto il suo territorio tranne che nel 2% dell’area 151.
La maggior parte dei santuari marini nazionali degli Stati Uniti è protetta in modo analogo dallo sfruttamento di petrolio e gas 240 [questo fino al 2026, quando l’amministrazione Trump ha dato il via ad un piano di espansione delle attività petrolifere offshore nei mari dell’Alaska, California e Golfo del Messico, mettendo a rischio anche le aree protette. NdR]. Il Papahānaumokuākea Marine National Monument alle Hawaii è la più grande area di conservazione contigua e completamente protetta sotto giurisdizione americana e una delle più grandi AMP al mondo con un’area di 1.508.870 km, nella quale è vietata qualsiasi attività di esplorazione, sviluppo o  produzione di petrolio, gas o minerali 241. In Australia, il parco marino della Grande Barriera Corallina (344.400 km²) è stato completamente protetto dallo sfruttamento offshore di petrolio e gas sin dalla sua istituzione nel 1975.242
produzione di petrolio, gas o minerali 241. In Australia, il parco marino della Grande Barriera Corallina (344.400 km²) è stato completamente protetto dallo sfruttamento offshore di petrolio e gas sin dalla sua istituzione nel 1975.242
Attraverso gli sforzi per eliminare gradualmente l’uso di petrolio e gas, questi paesi stanno anche proteggendo i propri mari e la vita marina.
Conclusione: i nostri mari del futuro
Le decisioni relative al petrolio e al gas offshore non riguardano solo il loro contributo significativo e a lungo termine alle emissioni di gas serra, ma anche la salute dei nostri mari, belli e ricchi di biodiversità, essenziali per la regolazione del clima. Continuare a concedere licenze e ad approvare nuove attività di produzione di petrolio e gas comporta una serie di impatti devastanti sui mari del Regno Unito che si protrarranno per decenni e che potrebbero lasciare un'eredità negativa molto più duratura sui nostri ecosistemi marini. I benefici che il Regno Unito trae da mari sani vanno ben oltre il sostentamento della pesca, spaziando dai nuovi composti per uso farmaceutico 243 alle attività ricreative 244 e al benessere 245, fino alla protezione delle nostre coste dall'erosione 14. Attualmente è in corso una vasta gamma di iniziative volte a investire in mari più sani nel Regno Unito, istituendo aree marine protette e rafforzando le aree dedicate alla loro protezione, al ripristino e alla rinaturalizzazione. Inoltre, aiutando la natura a ricostituire le barriere di ostriche e le praterie di fanerogame marine che abbiamo perso, migliorando la gestione della pesca, innovando per ridurre l'impatto della pesca a strascico e della dragaggio, e sviluppando un'acquacoltura sostenibile. Tutte queste azioni saranno compromesse dai nuovi progetti di estrazione di petrolio e gas in mare aperto, e non solo nei prossimi anni, ma per decenni.
Le evidenze scientifiche e le raccomandazioni delle Nazioni Unite e degli scienziati di tutto il mondo concordano sul fatto che una vera protezione degli oceani è essenziale per la vita umana e per la regolazione del clima. Bloccare il rilascio di licenze e l’approvazione di nuovi progetti di estrazione di petrolio e gas in mare aperto rappresenterebbe anche un enorme sostegno all’impegno del governo britannico a favore della conservazione marina e della protezione della biodiversità.
I mari del Regno Unito
possono essere stati pesantemente influenzati e modificati,
ma sono ancora ricchi e belli
e contengono oasi di meraviglia e diversità.
È importante sottolineare che hanno ancora la capacità di tornare ad essere le acque ricche di pesci, sostenute da barriere coralline rigogliose, che abbiamo avuto storicamente. L’oceano è già fondamentale per mitigare gli effetti peggiori del cambiamento climatico 18. Oltre il 90% del calore intrappolato dall’aumento dell’anidride carbonica viene assorbito dall’oceano, così come il 25-30% dell’anidride carbonica che altrimenti rimarrebbe nell’atmosfera causando un ulteriore riscaldamento. Senza questa capacità, oggi ci troveremmo in una situazione molto peggiore.
Questa è la capacità di un oceano degradato di cui non ci siamo presi cura adeguatamente. Un oceano sano e ben protetto, con numerose riserve marine rigorosamente tutelate, con un ricorso minimo alla pesca a strascico e al dragaggio e con una significativa riduzione di tutti gli altri impatti sugli ecosistemi marini, offre un enorme potenziale per un maggiore stoccaggio di carbonio. Questo potenziale non ancora realizzato, che consentirebbe all’oceano di diventare uno strumento molto più efficace nella lotta ai cambiamenti climatici, sta ottenendo un riconoscimento sempre maggiore, alimentando le richieste di una protezione più efficace dell’oceano.
Il conflitto tra l'espansione dell'estrazione di petrolio e gas e la tutela della biodiversità marina è un fenomeno globale, poiché l'estrazione di idrocarburi ha un impatto sugli ecosistemi marini di tutto il mondo. Tuttavia, è raro che tali attività si svolgano sistematicamente all'interno di aree marine protette 246.
Per un paese che si proclama leader mondiale nell'azione per il clima e nella conservazione marina, questa mancanza di coerenza è sconcertante ed è giunto il momento che l'opinione pubblica sia maggiormente consapevole di questo problema. Fermare la costruzione di nuove infrastrutture e l'estrazione petrolifera e del gas ridurrà i problemi che stiamo accumulando per le generazioni future. Si tratta di un impegno a lungo termine in termini di emissioni e infrastrutture, rumore e inquinamento, problematiche di smantellamento costose e complesse e, di conseguenza, una lunga lista di impatti sul nostro ambiente marino.
Figura 14. Le molteplici minacce che incombono sull'oceano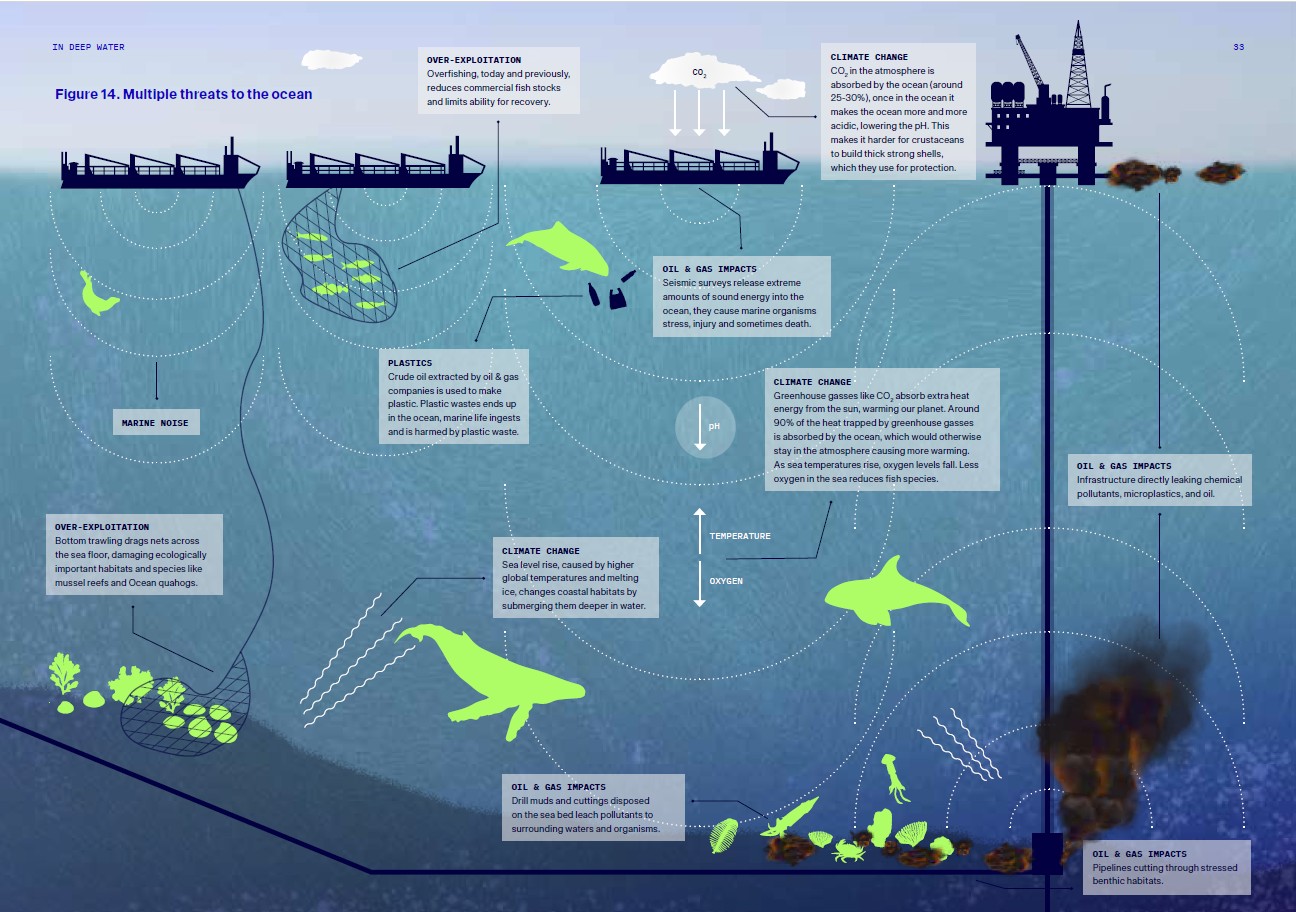
Considerata l'ampia gamma di impatti sugli ecosistemi marini
associati alle attività petrolifere e del gas offshore,
oltre alle devastanti conseguenze climatiche
derivanti dal proseguimento dell'estrazione di combustibili fossili,
la raccomandazione politica prioritaria
è quella di sospendere il rilascio di licenze e
l'approvazione di nuovi progetti di estrazione di petrolio e gas
offshore nelle acque del Regno Unito.
Questo consiglio è sostenuto dalle linee guida dell'Agenzia internazionale per l'energia 4 e da un'ampia gamma di analisi britanniche e globali. Sospendere il rilascio di licenze per nuovi progetti di estrazione di petrolio e gas offshore nel Regno Unito andrà a beneficio dell'azione internazionale per il clima e della reputazione internazionale del Regno Unito. L'attuale situazione, con centinaia di nuove licenze concesse e decine di nuovi impianti petroliferi e di gas in attesa di approvazione o che entreranno in funzione nei prossimi anni, è del tutto incompatibile con un futuro sano per i nostri mari. Tutte le nostre aree marine devono essere ben gestite per sostenerci e supportarci in un futuro incerto, ma è particolarmente importante che il governo del Regno Unito intensifichi la protezione dei nostri siti più diversificati e produttivi, molti dei quali rientrano nella nostra rete di aree marine protette (MPA).
I mari che circondano il Regno Unito sono meravigliosi, variegati e ricchi di vita, e costituiscono una parte fondamentale delle soluzioni climatiche (13, 247). Tuttavia, invece di rispettare gli impegni nazionali e internazionali per la conservazione degli oceani, con ogni nuova concessione petrolifera e di gas questi mari stanno diventando sempre più industrializzati e si trasformano in luoghi troppo rumorosi, troppo inquinati, troppo urbanizzati e troppo disturbati perché la nostra fauna marina possa prosperare.
Consentire nuovi progetti offshore di petrolio e gas non ridurrà le nostre bollette energetiche né aumenterà la nostra sicurezza energetica. Porterà alla costruzione di ulteriori infrastrutture e genererà maggiori emissioni, in contrasto con gli impegni climatici nazionali e globali. Impegnarci a fermare questo settore in rapida obsolescenza ci consentirà di recuperare i nostri ecosistemi marini, comprese aree marine protette (AMP) meglio gestite e una pesca più sostenibile, dando priorità all’energia rinnovabile e ripristinando i mari ricchi e meravigliosi a cui tutti aspiriamo.
CASI DI STUDIO: LE AREE MARINE PROTETTE
Le aree marine protette (AMP) dovrebbero rappresentare alcune delle nostre zone marine più pregiate e altamente protette, dove la vita marina possa prosperare, al riparo dall’impatto umano, e dove si possano mantenere gli impegni governativi per mari puliti, sani, ricchi di biodiversità e produttivi, a sostegno delle persone e della natura 299. Sebbene molte persone siano ormai consapevoli degli impatti diffusi di metodi di pesca distruttivi come la pesca a strascico e il dragaggio nelle Aree Marine Protette 300, pochissimi comprendono la portata delle attività petrolifere e del gas in questi luoghi, o gli effetti diretti e indiretti che l'estrazione di combustibili fossili sta avendo sui nostri luoghi oceanici più importanti.
Figura 15. Impatti del petrolio e del gas sulle caratteristiche e sul funzionamento dell'area marina protetta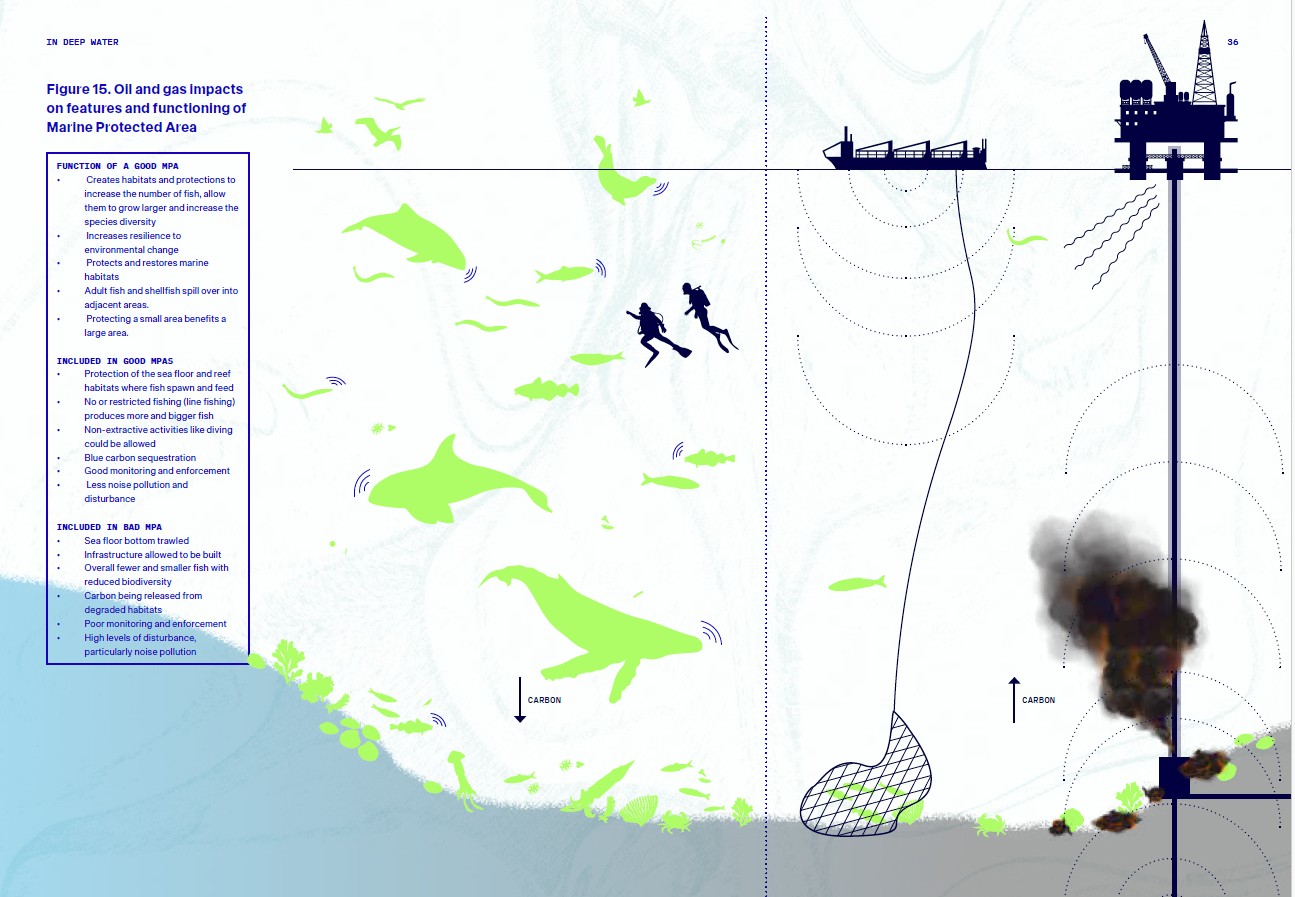
Zona speciale di conservazione (ZSC) del Dogger Bank
La Zona speciale di conservazione (ZSC) del Dogger Bank è un banco sabbioso ricco, produttivo e unico nel suo genere 301 nel Mare del Nord, che da secoli ospita popolazioni di anguille di sabbia e di pesci di importanza commerciale 302. Essa si sovrappone in gran parte alla ZSC del Mare del Nord meridionale (303), istituita per proteggere le popolazioni di focene 303. È considerata una parte particolarmente importante della rete di AMP del Regno Unito perché è la più grande distesa di sabbia nelle acque del paese, che comprende oltre il 70% dell’habitat dei banchi di sabbia del Regno Unito, e la sua formazione glaciale rende le sua caratteristiche particolarmente interessanti 304. Nel 2022 la pesca a strascico e il dragaggio sono stati vietati nell’AMP 144, migliorando la protezione offerta all’habitat del banco di sabbia.
Grazie a questa protezione, potrebbe essere possibile il recupero di specie attualmente rare, tra cui la razza chiodata (Raja Clavata) 305. Tuttavia, le attuali e future attività petrolifere e di estrazione del gas compromettono la protezione esistente e futura e riducono drasticamente i benefici che potrebbero derivare dal divieto di pesca con reti mobili.
All’interno dei confini dell’Area Speciale
di Conservazione del Dogger Bank,
la nostra analisi ha evidenziato la presenza di 176 pozzi,
13 piattaforme e una rete di 633 km di condotte associate.
La vita marina associata all’habitat del banco di sabbia comprende vermi, anfipodi, bivalvi, granchi, pesci piatti e fitti aggregati di ofiuroidi 306. Vi sono aree di coralli molli, briozoi ramificati (cerfoglio di mare) e costruttori di barriera [corallina] tubiformi (serpulidi) 307. Le anguille di sabbia sostengono un ecosistema diversificato, specie preda per le foche grigie e le foche comuni (308), per le focene,303 309 e per molte specie di uccelli marini. Qui si trovano anche le vongole oceaniche 306. Anche le balenottere minori, i globicefali, i tursiopi, i delfini comuni, i delfini dal becco bianco e i delfini dal fianco bianco dell'Atlantico utilizzano l'area 310.
La Zona speciale di conservazione del Dogger Bank è già fortemente interessata dall’industria offshore dei combustibili fossili. All’interno dei confini della ZSC, la nostra analisi ha evidenziato la presenza di 176 pozzi, 13 piattaforme e una rete di 633 km di condotte associate. L’impronta fisica stimata delle infrastrutture relative a piattaforme e pozzi è pari a 0,188 km². L’area stimata interessata dai detriti di perforazione associati a questi pozzi e piattaforme è di 71 km² 311.
Per quanto riguarda l'impatto del rumore sui cetacei, ci concentriamo sui potenziali impatti sulle focene, in quanto elemento caratteristico designato della ZSC del Mare del Nord meridionale 303. Le focene sono particolarmente sensibili ai disturbi [causati dal rumore] e vulnerabili, poiché il loro elevato tasso metabolico, le dimensioni ridotte e le scarse riserve di grasso rendono le risposte comportamentali potenzialmente gravose 75,77.
Laddove i disturbi aumentano il fabbisogno energetico o riducono l'efficienza nel procurarsi il cibo, sussiste il rischio di effetti significativi sulla sopravvivenza a livello sia individuale che di popolazione 95. Nelle focene sono state osservate risposte comportamentali e fisiologiche sia ai rumori antropogenici continui che a quelli impulsivi 312, 77). Dopo l’installazione di rilevatori di ecolocalizzazione sul Dogger Bank presso una piattaforma di gas offshore - prima, durante e dopo la costruzione - abbinati a rilevatori in siti di controllo per monitorare l’attività delle focene 255, è stato segnalato lo sfollamento e un’attività delle focene significativamente inferiore durante la fase di perforazione e costruzione (durata un anno), con un ritorno dell’attività ai livelli di base cinque mesi dopo la costruzione.
ecolocalizzazione sul Dogger Bank presso una piattaforma di gas offshore - prima, durante e dopo la costruzione - abbinati a rilevatori in siti di controllo per monitorare l’attività delle focene 255, è stato segnalato lo sfollamento e un’attività delle focene significativamente inferiore durante la fase di perforazione e costruzione (durata un anno), con un ritorno dell’attività ai livelli di base cinque mesi dopo la costruzione.
Area Marina Protetta per la Conservazione della Natura di Gannet e Montrose
La zona est dell'Area Marina Protetta per la Conservazione della Natura di Gannet e Montrose è importante per la presenza della vongola oceanica e di insoliti habitat fangosi di acque profonde, ma entrambe queste caratteristiche sono in cattive condizioni 313. Ciò non sorprende, dato che il sito è ampiamente utilizzato per l'estrazione offshore di petrolio e gas 314.
Anziché impegnarsi per il recupero del sito nell'ambito dell'ultimo round di concessioni 315, sono attualmente in fase di offerta nuove aree per lo sviluppo di petrolio e gas, il che comporterà ulteriori effetti negativi. L'AMP è stata proposta per la protezione degli aggregati di vongole oceaniche e dei fondali fangosi di acque profonde offshore 314. Sono inclusi fra gli elementi protetti anche gli habitat di sabbia e di ghiaia al largo in acque subtidali a profondità comprese tra 80 e 100 m, adatti alla colonizzazione da parte delle vongole oceaniche 316. I fondali fangosi di acque profonde offshore sono uno dei pochi esempi del loro genere influenzati dall’Atlantico sulla piattaforma continentale nella regione 317, e questa è l’unica MPA nel Mare del Nord settentrionale designata per proteggere i fondali fangosi di acque profonde offshore 318, sempre più riconosciuti per il loro valore in termini di carbonio blu 173.
Nella parte settentrionale e occidentale dell’AMP è presente un’intensa attività legata agli idrocarburi.
Si contano in totale 225 pozzi, 4 piattaforme e 827 km di condotte. L’impronta fisica stimata delle infrastrutture relative alle piattaforme e ai pozzi è pari a 0,179 km². L’area stimata interessata dai detriti di perforazione associati a questi pozzi e piattaforme è di 55 km².
Si ritiene che questa infrastruttura abbia probabilmente influito sulle popolazioni di vongole oceaniche nell’AMP 313. Il recupero delle popolazioni [di vongole] sarà probabilmente estremamente lento, dell’ordine di secoli 313. Si ritiene che le acque del Regno Unito fungano da bacino di raccolta per la specie, con larve provenienti dalle acque islandesi e lunghi periodi tra un evento di selezione riuscito e l’altro. È quindi importante che l’abbondanza e la struttura per età siano conservate a lungo termine per mantenere la popolazione all’interno del sito 313.
Sebbene i cetacei non siano fra gli elementi caratteristici designati dell’AMP, vi è la possibilità di impatti acustici sulle specie di cetacei, protette dalla legge in tutte le acque del Regno Unito. Sulla base della loro distribuzione e delle osservazioni, le focene, i delfini dal becco bianco, i delfini dal fianco bianco dell’Atlantico, i tursiopi e le balenottere minori sono le specie più suscettibili di subire l’impatto del rumore nell’AMP 322–324. In tutto questo sito è stato segnalato un elevato livello di attività di prospezione sismica, con implicazioni per i mammiferi marini e altre specie.
Area marina protetta per la conservazione della natura della “Faroe-Shetland Sponge Belt”
Questa vasta area marina protetta (AMP) è un punto nevralgico di importanza internazionale per la biodiversità, ospita diverse colonie di spugne ed è frequentata da globicefali, delfini dal fianco bianco dell'Atlantico e molti altri mammiferi marini stanziali e migratori 298. Le attività di esplorazione ed estrazione di idrocarburi sono in corso nel Canale delle Isole Faroe-Shetland dall'inizio degli anni '90 22 e gran parte di questa area marina protetta è attualmente oggetto dell'ultimo ciclo di concessioni 315, il che minaccia un'ulteriore perdita di habitat, disturbi e inquinamento. L'AMP per la conservazione della natura della “Faroe-Shetland Sponge Belt” ospita diverse comunità di spugne ostur boreali, uniche al mondo, ed è classificata come Ecosistema Marino Vulnerabile, di valore e interesse internazionale 266. Queste spugne creano habitat ricchi e produttivi per molte altre specie in via di estinzione, tra cui squali, razze e chimere 261,264. Sono importanti nel ciclo dei nutrienti oceanici 325, e probabilmente saranno importanti per la pesca 263.
Oltre alle comunità di spugne, le principali caratteristiche ecologiche per la designazione [dell’ Area come AMP] sono gli aggregati di vongole oceaniche e le sabbie e ghiaie subtidali al largo. Lo stato di conservazione di tutte queste caratteristiche è classificato come sfavorevole. L'area è interessante dal punto di vista oceanografico, dove le calde acque dell'Atlantico si sovrappongono alle fredde acque del Mare di Norvegia 326 creando un gradiente termico estremo e variabile che influenza la biodiversità della vita marina nella zona 327. Altre specie di interesse per la conservazione includono anemoni, coralli a coppa, pennatulacei e coralli molli, nonché curiosità oceaniche tra cui ragni di mare con un'apertura delle zampe di 40 cm ed enormi stelle a cestello, parenti delle normali stelle marine ma con braccia ultra-ramificate con oltre 5000 punte 328.
Video 
Il Canale delle Isole Faroe-Shetland è ben noto per l'abbondanza di grandi balene e delfini (329,330,331). Si ritiene che le balenottere comuni siano migratorie stagionali e visitatrici estive, e si registrano anche avvistamenti occasionali di balene blu, balenottere boreali e megattere. Le balene pilota a pinna lunga, i delfini dal fianco bianco dell'Atlantico, i delfini dal becco bianco e le focene sono tutti comuni nell'AMP. Le attività petrolifere e del gas sono già in corso in prossimità di queste aree di interesse conservazionistico 263. All'interno dei confini dell'AMP della Faroe-Shetland Sponge Belt, ci sono 285 pozzi, 543 km di condotte e attualmente nessuna piattaforma. L'impronta fisica stimata dell'infrastruttura dei pozzi è di 0,29 km2. L'area stimata interessata dai detriti di perforazione associati a questi pozzi è di 57 km2. Uno studio sul giacimento di Laggan, situato all'interno dell'MPA, ha evidenziato un impatto significativo sull'ecologia dei fondali marini dopo la perforazione, e un recupero solo parziale dopo 10 anni 74. La costruzione e la gestione delle infrastrutture petrolifere hanno un impatto visibile sulla distribuzione delle specie marine, che è stata studiata utilizzando immagini dei fondali 332.
(5. Fine)
* Traduzione di Ecor.Network
In Deep Water: Exposing the hidden impacts of oil and gas on the UK’s seas
Oceana, Uplift
Aprile 2023, 45 pp.
Download:

Note:
1. Galparsoro, I. et al. Reviewing the ecological impacts of offshore wind farms. npj Ocean Sustainability 1, 1 (2022).
2. Marappan, S., Stokke, R., Malinovsky, M.P., & Taylor, A. Assessment of impacts of the offshore oil and gas industry on the marine environment. in OSPAR, 2023: The 2023 Quality Status Report for the North-East Atlantic. (OSPAR Commission, 2022).
3. Welsby, D., Price, J., Pye, S. & Ekins, P. Unextractable fossil fuels in a 1.5 °C world. Nature 597, 230–234 (2021).
4. IEA. Net Zero by 2050. https://www.iea.org/reports/net-zero-by-2050 (2021).
5. BEIS/Prime Minister’s Office. UK enshrines new target in law to slash emissions by 78% by 2035. https://www.gov.uk/government/news/uk-enshrines-new-target-in-law-to-slash-emissions-by-78-by-2035 (2021).
6. UNFCCC. The Paris Agreement. https://unfccc.int/process-and-meetings/the-paris-agreement/the-paris-agreement (Undated).
7. Supran, G., Rahmstorf, S. & Oreskes, N. Assessing ExxonMobil’s global warming projections. Science 379, eabk0063.
8. Franta, B. Early oil industry disinformation on global warming. Environmental Politics 30, 663–668 (2021).
9. ExxonMobil. https://www.exxonmobil.co.uk/company/overview/uk-operations/production. (2019).
10. McCauley, D. J. et al. Marine defaunation: Animal loss in the global ocean. Science 347, 1255641 (2015).
11. Worm, B. et al. Impacts of Biodiversity Loss on Ocean Ecosystem Services. Science 314, 787–790 (2006).
12. Palumbi, S. R. et al. Managing for ocean biodiversity to sustain marine ecosystem services. Frontiers in Ecology and the Environment 7, 204–211 (2009).
13. Hoegh-Guldberg, O. et al. The ocean as a solution to climate change: Five opportunities for action. (2019).
14. Smale, D. A., Burrows, M. T., Moore, P., O’Connor, N. & Hawkins, S. J. Threats and knowledge gaps for ecosystem services provided by kelp forests: a northeast Atlantic perspective. Ecology and Evolution 3, 4016–4038 (2013).
15. Ondiviela, B. et al. The role of seagrasses in coastal protection in a changing climate. Coastal Engineering 87, 158–168 (2014).
16. Bloor, I. S. M. et al. Boom not bust: Cooperative management as a mechanism for improving the commercial efficiency and environmental outcomes of regional scallop fisheries. Marine Policy 132, 104649 (2021).
17. Avdelas, L. et al. The decline of mussel aquaculture in the European Union: causes, economic impacts and opportunities. Reviews in Aquaculture 13, 91–118 (2021).
18. Hoegh-Guldberg, O., Northrop, E. & Lubchenco, J. The ocean is key to achieving climate and societal goals. Science 365, 1372–1374 (2019).
19. Laffoley, D. et al. The forgotten ocean: Why COP26 must call for vastly greater ambition and urgency to address ocean change. Aquatic Conservation: Marine and Freshwater Ecosystems 32, 217–228 (2022).
20. Roberts, C. M. et al. Marine reserves can mitigate and promote adaptation to climate change. Proc Natl Acad Sci USA 114, 6167 (2017).
21. Duarte, C. M. et al. Rebuilding marine life. Nature 580, 39–51 (2020).
22. Vad, J. et al. Chapter Two - Potential Impacts of Offshore Oil and Gas Activities on Deep-Sea Sponges and the Habitats They Form. in Advances in Marine Biology (ed. Sheppard, C.) vol. 79 33–60 (Academic Press, 2018).
23. Animah, I. & Shafiee, M. Condition assessment, remaining useful life prediction and life extension decision making for offshore oil and gas assets. Journal of Loss Prevention in the Process Industries 53, 17–28 (2018).
24. Hjorth, M. et al. Effects of Oil and Gas Production On Marine Ecosystems and Fish Stocks in the Danish North Sea: Review. Report for WSP Denmark. https://mst.dk/media/222352/oil_gas-effect-report_final.pdf (2021).
25. Stowe, T. J. & Underwood, L. A. Oil spillages affecting seabirds in the United Kingdom, 1966–1983. Marine Pollution Bulletin 15, 147–152 (1984).
26. Moore, J., Taylor, P. & Hiscock, K. Rocky shores monitoring programme. Proceedings of the Royal Society of Edinburgh. Section B. Biological Sciences 103, 181–200 (1995).
27. Riddick, S. N. et al. Methane emissions from oil and gas platforms in the North Sea. Atmospheric Chemistry and Physics 19, 9787–9796 (2019).
28. Cordes, E. E. et al. Environmental Impacts of the Deep-Water Oil and Gas Industry: A Review to Guide Management Strategies. Frontiers in Environmental Science 4, (2016).
29. Frost, K. J. et al. Alaska, and Adjacent Areas Following the Exxon Valdez Oil Spill Marine Mammal Study Number 5. (1994).
30. Garrott, R. A., Eberhardt, L. L. & Burn, D. M. Mortality of sea otters in Prince William Sound following the Exxon Valdez oil spill. Marine Mammal Science 9, 343–359 (1993).
31. Kerr, R., Kintisch, E. & Stokstad, E. Will Deepwater Horizon Set a New Standard for Catastrophe? Science 328, 674–675 (2010).
32. Montagna, P. A. et al. Deep-Sea Benthic Footprint of the Deepwater Horizon Blowout. PLOS ONE 8, e70540 (2013).
33. Bodkin JL et al. Long-term effects of the Exxon Valdez oil spill: sea otter foraging in the intertidal as a pathway of exposure to lingering oil. Mar Ecol Prog Ser 447, 273–287 (2012).
34. Heintz, R. A., Short, J. W. & Rice, S. D. Sensitivity of fish embryos to weathered crude oil: Part II. Increased mortality of pink salmon (Oncorhynchus gorbuscha) embryos incubating downstream from weathered Exxon valdez crude oil. Environmental Toxicology and Chemistry 18, 494–503 (1999).
35. Matkin, C. O., Saulitis, E. L., Ellis, G. M., Olesiuk, P. & Rice, S. D. Ongoing population-level impacts on killer whales Orcinus orca following the ‘Exxon Valdez’ oil spill in Prince William Sound, Alaska. Marine Ecology Progress Series 356, 269–281 (2008).
36. Muehlenbachs, L., Cohen, M. A. & Gerarden, T. The impact of water depth on safety and environmental performance in offshore oil and gas production. Energy Policy 55, 699–705 (2013).
37. Gallego, A. et al. Current status of deepwater oil spill modelling in the Faroe-Shetland Channel, Northeast Atlantic, and future challenges. Marine Pollution Bulletin 127, 484–504 (2018).
38. Jernelov, A. The threats from oil spills: now, then, and in the future. Ambio 39, 353–366 (2010).
39. Moore, J. et al. SEA EMPRESS SPILL: IMPACTS ON MARINE AND COASTAL HABITATS. International Oil Spill Conference Proceedings 1997, 213–216 (1997).
40. Banks, A. N. et al. The Sea Empress oil spill (Wales, UK): Effects on Common Scoter Melanitta nigra in Carmarthen Bay and status ten years later. Marine Pollution Bulletin 56, 895–902 (2008).
41. Webster, L. et al. Long-term Monitoring of Polycyclic Aromatic Hydrocarbons in Mussels (Mytilus edulis) Following the Braer Oil Spill†. Analyst 122, 1491–1495 (1997).
42. Conroy, J. & Kruuk, H. Changes in Otter Numbers in Shetland Between 1988 and 1993. Oryx vol. 29 197–204 (1995).
43. Hall, A. J., Watkins, J. & Hiby, L. The impact of the 1993 Braer oil spill on grey seals in Shetland. Science of The Total Environment 186, 119–125 (1996).
44. Goodlad, J. Effects of the Braer oil spill on the Shetland seafood industry. Science of The Total Environment 186, 127–133 (1996).
45. Equinor. Rosebank Environmental Statement ES/2022/001.
https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/1097880/Rosebank_Environmental_Statement_-_Final_for_Submission_To_OPRED_Equinor_3rd_August_2022.pdf (2022).
46. Baker, J. R., Jones, A. M., Jones, T. P. & Watson, H. C. Otter Lutra lutra L. mortality and marine oil pollution. Biological Conservation 20, 311–321 (1981).
47. Joye, S. B. et al. The Gulf of Mexico ecosystem, six years after the Macondo oil well blowout. Deep Sea Research Part II: Topical Studies in Oceanography 129, 4–19 (2016).
48. Law, R. J. & Hellou, J. Contamination of Fish and Shellfish Following Oil Spill Incidents. Environmental Geosciences 6, 90–98 (1999).
49. Bakhmet, I., Fokina, N. & Ruokolainen, T. Changes of Heart Rate and Lipid Composition in Mytilus Edulis and Modiolus Modiolus Caused by Crude Oil Pollution and Low Salinity Effects. J Xenobiot 11, 46–60 (2021).
50. Farinas-Franco, J. M. et al. Are we there yet? Management baselines and biodiversity indicators for the protection and restoration of subtidal bivalve shellfish habitats. Science of The Total Environment 863, 161001 (2023).
51. DeLeo, D. M., Ruiz-Ramos, D. V., Baums, I. B. & Cordes, E. E. Response of deep-water corals to oil and chemical dispersant exposure. Deep Sea Research Part II: Topical Studies in Oceanography 129, 137–147 (2016).
52. DeLeo, D. M., Lengyel, S. D. & Cordes, E. E. Assessing Oil Spill Impacts to Cold-Water Corals of the Deep Gulf of Mexico. 2016, PO13F-05 (2016).
53. OSPAR. Assessment of the OSPAR Report on Discharges, Spills and Emissions from Offshore Installations 2009 – 2018.
54. OSPAR. OSPAR report on discharges, spills and emissions from offshore oil and gas installations in 2012.
55. Dong, Y., Liu, Y., Hu, C., MacDonald, I. R. & Lu, Y. Chronic oiling in global oceans. Science 376, 1300–1304 (2022).
56. Camphuysen, K. C. J. Declines in oil-rates of stranded birds in the North Sea highlight spatial patterns in reductions of chronic oil pollution. Marine Pollution Bulletin 60, 1299–1306 (2010).
57. Camphuysen, K. & Heubeck, M. Beached Bird Surveys in the North Sea as an Instrument to Measure Levels of Chronic Oil Pollution. In Oil Pollution in the North Sea (ed. Carpenter, A.) 193–208 (Springer International Publishing, 2016). doi:10.1007/698_2015_435.
58. Neff, J., Lee, K. & DeBlois, E. M. Produced Water: Overview of Composition, Fates, and Effects. in Produced Water: Environmental Risks and Advances in Mitigation Technologies (eds.Lee, K. & Neff, J.) 3–54 (Springer New York, 2011). doi:10.1007/978-1-4614-0046-2_1.
59. OSPAR. Report on impacts of discharges of oil and chemicals in produced water on the marine environment. https://www.ospar.org/documents?v=47303 (2021).
60. Bakke, T., Klungsoyr, J. & Sanni, S. Environmental impacts of produced water and drilling waste discharges from the Norwegian offshore petroleum industry. Marine Environmental Research 92, 154–169 (2013).
61. Hansen, B. H. et al. Embryonic exposure to produced water can cause cardiac toxicity and deformations in Atlantic cod (Gadus morhua) and haddock (Melanogrammus aeglefinus) larvae. Marine Environmental Research 148, 81–86 (2019).
62. Meier, S. et al. DNA damage and health effects in juvenile haddock (Melanogrammus aeglefinus) exposed to PAHs associated with oil-polluted sediment or produced water. PLOS ONE 15, e0240307 (2020).
63. Neff, J. M. Polycyclic aromatic hydrocarbons in the aquatic environment. Biol. Conserv.;(United Kingdom) 18, (1980).
64. Tuvikene, A. Responses of fish to polycyclic aromatic hydrocarbons (PAHs). Annales Zoologici Fennici 32, 295–309 (1995).
65. Sundt, R. C., Pampanin, D. M., Grung, M., Baršienė, J. & Ruus, A. PAH body burden and biomarker responses in mussels (Mytilus edulis) exposed to produced water from a North Sea oil field: Laboratory and field assessments. Marine Pollution Bulletin 62, 1498–1505 (2011).
66. Capuzzo, J. M., Lancaster, B. A. & Sasaki, G. C. The effects of petroleum hydrocarbons on lipid metabolism and energetics of larval development and metamorphosis in the american lobster (homarus americanus Milne Edwards). Marine Environmental Research 14, 201–228 (1984).
67. Kho, F. et al. Current understanding of the ecological risk of mercury from subsea oil and gas infrastructure to marine ecosystems. Journal of Hazardous Materials 438, 129348 (2022).
68. Al-Kindi, S., Al-Bahry, S., Al-Wahaibi, Y., Taura, U. & Joshi, S. Partially hydrolyzed polyacrylamide: enhanced oil recovery applications, oil-field produced water pollution, and possible solutions. Environmental Monitoring and Assessment 194, 875 (2022).
69. Xiong, B. et al. Polyacrylamide degradation and its implications in environmental systems. npj Clean Water 1, 1–9 (2018).
70. Cruz, A. M. & Krausmann, E. Vulnerability of the oil and gas sector to climate change and extreme weather events. Climatic Change 121, 41–53 (2013).
71. Santos, M. F. L., Lana, P. C., Silva, J., Fachel, J. G. & Pulgati, F. H. Effects of non-aqueous fluids cuttings discharge from exploratory drilling activities on the deep-sea macrobenthic communities. Deep Sea Research Part II: Topical Studies in Oceanography 56, 32–40 (2009).
72. Veltman, K., Huijbregts, M. A., Rye, H. & Hertwich, E. G. Including impacts of particulate emissions on marine ecosystems in life cycle assessment: The case of offshore oil and gas production. Integrated Environmental Assessment and Management 7, 678–686 (2011).
73. Taylor, J., Drewery, J., & Boulcott, P. 1218S Cruise Report: Monitoring survey of Faroe-Shetland Sponge Belt NCMPA, Rosemary Bank Seamount NCMPA and Wyville Thomson Ridge SAC, (2019).
74. Jones DOB, Gates AR, & Lausen B. Recovery of deep-water megafaunal assemblages from hydrocarbon drilling disturbance in the Faroe−Shetland Channel. Mar Ecol Prog Ser 461, 71–82 (2012).
75. Duarte, C. M. et al. The soundscape of the Anthropocene ocean. Science 371, eaba4658 (2021).
76. Krause, B. Voices of the wild: animal songs, human din, and the call to save natural soundscapes. (Yale University Press, 2015).
77. Williams, W.J., Curnick, D.J., & Deaville, R. (last). Identification of key species in the UK, with a focus on English waters, sensitive to underwater noise, (2021).
78. Chou, E., Southall, B. L., Robards, M. & Rosenbaum, H. C. International policy, recommendations, actions and mitigation efforts of anthropogenic underwater noise. Ocean & Coastal Management 202, 105427 (2021).
79. Rako-Gospi, N. & Picciulin, M. Chapter 20 - Underwater Noise: Sources and Effects on Marine Life. in World Seas: An Environmental Evaluation (Second Edition) (ed. Sheppard, C.) 367–389 (Academic Press, 2019).
80. Mooney, T. A., Andersson, M. H. & Stanley, J. Acoustic impacts of offshore wind energy on fishery resources. Oceanography 33, 82–95 (2020).
81. Nowacek, D. P. et al. Marine seismic surveys and ocean noise: time for coordinated and prudent planning. Frontiers in Ecology and the Environment 13, 378–386 (2015).
82. Erbe, C., Duncan, A., Hawkins, L., Terhune, J. M. & Thomas, J. A. Introduction to Acoustic Terminology and Signal Processing. in Exploring Animal Behavior Through Sound: Volume 1 111–152 (Springer, 2022).
83. Nieukirk, S. L. et al. Sounds from airguns and fin whales recorded in the mid-Atlantic Ocean, 1999–2009. The Journal of the Acoustical Society of America 131, 1102–1112 (2012).
84. McCauley, R. D. et al. Widely used marine seismic survey air gun operations negatively impact zooplankton. Nat Ecol Evol 1, 1–8 (2017).
85. Mann, D. et al. Hearing Loss in Stranded Odontocete Dolphins and Whales. PLOS ONE 5, e13824 (2010).
86. Kavanagh, A. S., Nykanen, M., Hunt, W., Richardson, N. & Jessopp, M. J. Seismic surveys reduce cetacean sightings across a large marine ecosystem. Sci Rep 9, 19164 (2019).
87. Castellote, M. & Llorens, C. Review of the Effects of Offshore Seismic Surveys in Cetaceans: Are Mass Strandings a Possibility? in The Effects of Noise on Aquatic Life II (eds. Popper, A. N. & Hawkins, A.) 133–143 (Springer New York, 2016).
88. Lucke, K., Siebert, U., Lepper, P. A. & Blanchet, M.-A. Temporary shift in masked hearing thresholds in a harbor porpoise (Phocoena phocoena) after exposure to seismic airgun stimuli. The Journal of the Acoustical Society of America 125, 4060–4070 (2009).
89. Pirotta, E., Brookes, K. L., Graham, I. M. & Thompson, P. M. Variation in harbour porpoise activity in response to seismic survey noise. Biology Letters 10, 20131090 (2014).
90. Gordon, J. C. D. et al. A Review of the Effects of Seismic Survey on Marine Mammals. Marine Technology Society Journal 37, (2003).
91. Stone, C. J. The effects of seismic activity on marine mammals in UK waters, 1998-2000, (2003).
92. Stone, C. J., Hall, K., Mendes, S. & Tasker, M. L. The effects of seismic operations in UK waters: analysis of Marine Mammal Observer data. Journal of Cetacean Research and Management (2017).
93. Dunlop, R. A. et al. The behavioural response of migrating humpback whales to a full seismic airgun array. Proceedings of the Royal Society B: Biological Sciences 284, 20171901 (2017).
94. McCauley, R. D. et al. MARINE SEISMIC SURVEYS— A STUDY OF ENVIRONMENTAL IMPLICATIONS. The APPEA Journal 40, 692–708 (2000).
95. Wisniewska, D. M. et al. Ultra-High Foraging Rates of Harbor Porpoises Make Them Vulnerable to Anthropogenic Disturbance. Current Biology 26, 1441–1446 (2016).
96. Nelms, S. E., Piniak, W. E. D., Weir, C. R. & Godley, B. J. Seismic surveys and marine turtles: An underestimated global threat? Biological Conservation 193, 49–65 (2016).
97. Soto, N. A. et al. Anthropogenic noise causes body malformations and delays development in marine larvae. Sci Rep 3, 1–5 (2013).
98. Guerra, A., Gonzalez, A. & Rocha, F. A review of records of giant squid in the north-eastern Atlantic and severe injuries in Architeuthis dux stranded after acoustic exploration. ICES CM 2004, (2004).
99. Sole, M., Monge, M., Andre, M. & Quero, C. A proteomic analysis of the statocyst endolymph in common cuttlefish (Sepia officinalis): an assessment of acoustic trauma after exposure to sound. Scientific Reports 9, 9340 (2019).
100. Day, R. D., McCauley, R. D., Fitzgibbon, Q. P., Hartmann, K. & Semmens, J. M. Seismic air guns damage rock lobster mechanosensory organs and impair righting reflex. Proceedings of the Royal Society B: Biological Sciences 286, 20191424 (2019).
101. Andre, M. et al. Low-frequency sounds induce acoustic trauma in cephalopods. Frontiers in Ecology and the Environment 9, 489–493 (2011).
102. Davidsen, J. G. et al. Effects of sound exposure from a seismic airgun on heart rate, acceleration and depth use in free-swimming Atlantic cod and saithe. Conservation Physiology 7, coz020 (2019).
103. Sierra-Flores, R., Atack, T., Migaud, H. & Davie, A. Stress response to anthropogenic noise in Atlantic cod Gadus morhua L. Aquacultural Engineering 67, 67–76 (2015).
104. Engas, A. & Lokkeborg, S. Effects of seismic shooting and vessel-generated noise on fish behaviour and catch rates. Bioacoustics 12, 313–316 (2002).
105. Lokkeborg, S., Ona, E., Vold, A. & Salthaug, A. Sounds from seismic air guns: gear- and species-specific effects on catch rates and fish distribution. Can. J. Fish. Aquat. Sci. 69, 1278–1291 (2012).
106. Slotte, A., Hansen, K., Dalen, J. & Ona, E. Acoustic mapping of pelagic fish distribution and abundance in relation to a seismic shooting area off the Norwegian west coast. Fisheries Research 67, 143–150 (2004).
107. Hassel, A. et al. Reaction of sand eel to seismic shooting: A field experiment and fishery statistics study. (2003).
108. Hassel, A. et al. Influence of seismic shooting on the lesser sandeel (Ammodytes marinus). ICES Journal of Marine Science - ICES J MAR SCI 61, 1165–1173 (2004).
109. Merchant, N. D. & Robinson, S. Abatement of underwater noise pollution from pile-driving and explosions in UK waters. in vol. 12 (2019).
110. Dahne, M. et al. Effects of pile-driving on harbour porpoises (Phocoena phocoena) at the first offshore wind farm in Germany. Environmental Research Letters 8, 025002 (2013).
111. Genesis Oil and Gas & Consultants. Review and Assessment of Underwater Sound Produced from Oil and Gas Sound Activities and Potential Reporting Requirements under the Marine Strategy Framework Directive, (2011).
112. Fowler, A. M. et al. Environmental benefits of leaving offshore infrastructure in the ocean.Frontiers in Ecology and the Environment 16, 571–578 (2018).
113. MacIntosh, A., Dafforn, K., Penrose, B., Chariton, A. & Cresswell, T. Ecotoxicological effects of decommissioning offshore petroleum infrastructure: A systematic review. Critical Reviews in Environmental Science and Technology 52, 3283–3321 (2022).
114. Cantle, P. & Bernstein, B. Air emissions associated with decommissioning California’s offshore oil and gas platforms. Integrated Environmental Assessment and Management 11, 564–571 (2015).
115. Coolen, J. W. P. et al. Ecological implications of removing a concrete gas platform in the North Sea. Journal of Sea Research 166, 101968 (2020).
116. Stap, T., Coolen, J. W. P. & Lindeboom, H. J. Marine Fouling Assemblages on Offshore Gas Platforms in the Southern North Sea: Effects of Depth and Distance from Shore on Biodiversity. PLOS ONE 11, e0146324 (2016).
117. Ahiaga-Dagbui, D., Whyte, A. & Boateng, P. Costing and Technological Challenges of Offshore Oil and Gas Decommissioning in the UK North Sea. Journal of Construction Engineering and Management 143, (2017).
118. Jorgensen, D. OSPAR’s exclusion of rigs-toreefs in the North Sea. Ocean & Coastal Management 58, 57–61 (2012).
119. OSPAR. OSPAR Decision 98/3 on the Disposal of Disused Offshore Installations, (1998).
120. Fortune, I. S. & Paterson, D. M. Ecological best practice in decommissioning: a review of scientific research. ICES Journal of Marine Science 77, 1079–1091 (2020).
121. Tidbury, H. et al. Social network analysis as a tool for marine spatial planning: Impacts of decommissioning on connectivity in the North Sea. Journal of Applied Ecology 57, 566–577 (2020).
122. Ekins, P., Vanner, R. & Firebrace, J. Decommissioning of offshore oil and gas facilities: A comparative assessment of different scenarios. Journal of Environmental Management 79, 420–438 (2006).
123. Aslani, F., Zhang, Y., Manning, D., Valdez, L. C. & Manning, N. Additive and alternative materials to cement for well plugging and abandonment: A state-of-the-art review. Journal of PetroleumScience and Engineering 215, 110728 (2022).
124. North Sea Transition Authority (NSTA). UKCS Decommissioning Cost Estimate 2022, (2022).
125. Hegmann, G. et al. Cumulative Effects Assessment Practitioners Guide. (1999).
126. Kirkfeldt, T. S. et al. Why cumulative impacts assessments of hydrocarbon activities in the Arctic fail to meet their purpose. Reg Environ Change 17, 725–737 (2017).
127. Pirotta, E. et al. Understanding the combined effects of multiple stressors: A new perspective on a longstanding challenge. Science of The Total Environment 821, 153322 (2022).
128. Bindoff, N. L. et al. Changing ocean, marine ecosystems, and dependent communities. IPCC special report on the ocean and cryosphere in a changing climate 477–587 (2019).
129. Gissi, E. et al. A review of the combined effects of climate change and other local human stressors on the marine environment. Science of The Total Environment 755, 142564 (2021).
130. Jackson, E. L., Davies, A. J., Howell, K. L., Kershaw, P. J. & Hall-Spencer, J. M. Future-proofing marine protected area networks for cold water coral reefs. ICES Journal of Marine Science 71, 2621–2629 (2014).
131. Roberts, D. A. et al. Ocean acidification increases the toxicity of contaminated sediments. Global Change Biology 19, 340–351 (2013).
132. Willsteed, E., Gill, A. B., Birchenough, S. N. R. & Jude, S. Assessing the cumulative environmental effects of marine renewable energy developments: Establishing common ground. Science of The Total Environment 577, 19–32 (2017).
133. Laffoley, D. et al. Chapter 29 – Marine Protected Areas. in World Seas: An Environmental Evaluation (Second Edition) (ed. Sheppard, C.) 549–569 (Academic Press, 2019).
134. Roberts, C. M., Bohnsack, J. A., Gell, F., Hawkins, J. P. & Goodridge, R. Effects of Marine Reserves on Adjacent Fisheries. Science 294, 1920–1923 (2001).
135. Ban, N. C. et al. Well-being outcomes of marine protected areas. Nature Sustainability 2, 524–532 (2019).
136. Sheehan, E. V. et al. Rewilding of Protected Areas Enhances Resilience of Marine Ecosystems to Extreme Climatic Events. Frontiers in Marine Science 8, (2021).
137. Gell, F. R. & Roberts, C. M. Benefits beyond boundaries: the fishery effects of marine reserves. Trends in Ecology & Evolution 18, 448–455 (2003).
138. Convention on Biological Diversity. Final text of Kunming-Montreal Global Biodiversity Framework. (2022).
139. JNCC. UK Marine Protected Area Network Statistics, (2022).
140. North Sea Transition Authority (NSTA), Offshore Petroleum Licensing Rounds,(2022).
141. Guidelines for applying the IUCN protected area management categories to marine protected areas. (IUCN).
142. Stolton, S., Shadie, P., & Dudley, N. IUCN WCPA Best Practice Guidance on Recognising Protected Areas and Assigning Management Categories and Governance Types.
143. Burdon, D., Barnard, S., Boyes, S. J. & Elliott, M. Oil and gas infrastructure decommissioning in marine protected areas: System complexity, analysis and challenges. Marine Pollution Bulletin 135, 739–758 (2018).
144. Marine Management Organisation. The Dogger Bank Special Area of Conservation (Specified Area) Bottom Towed Fishing Gear Byelaw 2022, (2022).
145. JNCC. English Highly Protected Marine Areas. (2022).
146. Scottish Government. Highly Protected Marine Areas (HPMAs) - site selection: draft guidelines. / (2022).
147. Marine Conservation Society & Rewilding Britain. Marine Conservation Society & Rewilding Britain. (2022) Blue carbon: Ocean-based solutions to fight the climate crisis. A report by the Marine Conservation Society and Rewilding Britain. (2022).
148. Grorud-Colvert, K. et al. The MPA Guide: A framework to achieve global goals for the ocean. Science 373, eabf0861 (2021).
149. Santo, E. M. D. Assessing public participation in environmental decision-making: Lessons learned from the UK Marine Conservation Zone (MCZ) site selection process. Marine Policy 64, 91–101 (2016).
150. Engel, M. T. & Vaske, J. J. Balancing public acceptability and consensus regarding marine protected areas management using the Potential for Conflict Index2. Marine Policy 139, 105042 (2022).
151. Gies, Erica. Canada Has New Rules Governing Its Marine Protected Areas. Do They Go Far Enough? (2019).
152. DEFRA. Inner Silver Pit South: Consultation factsheet for candidate Highly Protected Marine Area (HPMA). (2022).
153. Gamble, C. et al. Seagrass Restoration Handbook: UK and Ireland. in (Zoological Society of London, 2021).
154. Fodrie, F. J. et al. Oyster reefs as carbon sources and sinks. Proceedings of the Royal Society B: Biological Sciences 284, 20170891 (2017).
155. Green, A. E., Unsworth, R. K. F., Chadwick, M. A. & Jones, P. J. S. Historical Analysis Exposes Catastrophic Seagrass Loss for the United Kingdom. Frontiers in Plant Science 12, (2021).
156. Lovelock, C. E. & Reef, R. Variable Impacts of Climate Change on Blue Carbon. One Earth 3, 195–211 (2020).
157. Climate Change Committee. Briefing: Blue Carbon-March 2022 Climate Change Committee. (2022).
158. Costa, M. & Macreadie, P. The Evolution of Blue Carbon Science. Wetlands 42, (2022).
159. Claes, J., Hopman, D., Jaeger, G. & Rogers, M. Blue carbon: The potential of coastal and oceanic climate action. (2022).
160. Macreadie, P. I. et al. Blue carbon as a natural climate solution. Nature Reviews Earth & Environment 2, 826–839 (2021).
161. Burden, Annette & Clilverd, Hannah. Moving towards inclusion of coastal wetlands in the UK LULUCF inventory: rapid assessment of activity data availability. 61 (2022).
162. Krause-Jensen, D. et al. Sequestration of macroalgal carbon: the elephant in the Blue Carbon room. Biology Letters 14, 20180236 (2018).
163. Cullen-Unsworth, L. C. & Unsworth, R. K. Strategies to enhance the resilience of the world’s seagrass meadows. Journal of Applied Ecology 53, 967–972 (2016).
164. Hiraishi, T. et al. 2013 supplement to the 2006 IPCC guidelines for national greenhouse gas inventories: Wetlands. IPCC, Switzerland (2014).
165. Austin, W., Smeaton, C., Houston, A. & Balke, T. Scottish saltmarsh, sea-level rise, and the potential for managed realignment to deliver blue carbon gains. (2022).
166. Smeaton, C. et al. Using citizen science to estimate surficial soil Blue Carbon stocks in Great British saltmarshes. Frontiers in Marine Science 461 (2022).
167. Boorman, L. Saltmarsh Review. An overview of coastal saltmarshes, their dynamic and sensitivity characteristics for conservation and management. (2003).
168. Davy, A., Bakker, J. & Figueroa, M. Human modification of European salt marshes. Human impacts on salt marshes: a global perspective. University of California Press, Berkeley, California, USA 311–336 (2009).
169. Jones, B. L. & Unsworth, R. K. F. The perilous state of seagrass in the British Isles. Royal Society Open Science 3, 150596.
170. Arias-Ortiz, A. et al. A marine heatwave drives massive losses from the world’s largest seagrass carbon stocks. Nature Climate Change 8, 338–344 (2018).
171. Porter, J. et al. Blue carbon audit of Orkney waters. (2020).
172. Austin, W., Turrell, W. & Tilbrook, C. A brief history of Scottish blue carbon science and the Scottish Blue Carbon Forum: Where next? in.
173. Burrows, M. et al. Assessment of carbon capture and storage in natural systems within the English North Sea (Including within Marine Protected Areas). (2021).
174. Mariani, G. et al. Let more big fish sink: Fisheries prevent blue carbon sequestration—half in unprofitable areas. Science Advances 6, eabb4848.
175. Pershing, A. J., Christensen, L. B., Record, N. R., Sherwood, G. D. & Stetson, P. B. The Impact of Whaling on the Ocean Carbon Cycle: Why Bigger Was Better. PLOS ONE 5, e12444 (2010).
176. Christianson, A. B. et al. The promise of blue carbon climate solutions: where the science supports ocean-climate policy. Frontiers in Marine Science 589 (2022).
177. Durfort, A. et al. Recovery of carbon benefits by overharvested baleen whale populations is threatened by climate change. Proceedings of the Royal Society B: Biological Sciences 289, 20220375 (2022).
178. Tulloch, V. J. D., Plaganyi, E. E., Brown, C., Richardson, A. J. & Matear, R. Future recovery of baleen whales is imperiled by climate change. Global Change Biology 25, 1263–1281 (2019).
179. Bijma, J., Portner, H.-O., Yesson, C. & Rogers, A. D. Climate change and the oceans – What does the future hold? Marine Pollution Bulletin 74, 495–505 (2013).
180. Wright, P., Pinnegar, J. & Fox, C. Impacts of climate change on fish, relevant to the coastal and marine environment around the UK. 354–381 (2020).
181. Gormley, K. et al. Connectivity and Dispersal Patterns of Protected Biogenic Reefs: Implications for the Conservation of Modiolus modiolus (L.) in the Irish Sea. PLOS ONE 10, e0143337 (2015).
182. Hiscock, K. Exploring Britain’s Hidden World: A Natural History of Seabed Habitats. (2018).
183. Edwards, M. et al. Plankton, jellyfish and climate in the North-East Atlantic. MCCIP Sci. Rev 2020, 322–353 (2020).
184. Fromentin JM & Planque B. Calanus and environment in the eastern North Atlantic. II. Influence of the North Atlantic Oscillation on C. finmarchicus and C. helgolandicus. Mar Ecol Prog Ser 134, 111–118 (1996).
185. Engelhard, G. H., Righton, D. A. & Pinnegar, J. K. Climate change and fishing: a century of shifting distribution in North Sea cod. Global Change Biology 20, 2473–2483 (2014).
186. Evans, P. G. H. & Waggitt, J. J. Impacts of climate change on marine mammals, relevant to the coastal and marine environment around the UK (MCCIP Science Review 2020).
187. Vezzulli, L. et al. Climate influence on Vibrio and associated human diseases during the past half-century in the coastal North Atlantic. Proceedings of the National Academy of Sciences 113, E5062–E5071 (2016).
188. Walsh, J. E. et al. The high latitude marine heat wave of 2016 and its impacts on Alaska. Bull. Am. Meteorol. Soc 99, S39–S43 (2018).
189. IPCC. Climate change 2014: Synthesis report. Contribution of working groups I, II and III to the Fifth Assessment Report of the Intergovernmental Panel on Climate Change [Core Writing Team, R.K. Pachauri and L.A. Meyer (eds.)]. 151 (2014).
190. Mahaffey, C., Palmer, M., Greenwood, N. & Sharples, J. Impacts of climate change on dissolved oxygen concentration relevant to the coastal and marine environment around the UK. MCCIP Science Review 31–53 (2020).
191. Smith, K. E. et al. Biological Impacts of Marine Heatwaves. Annu. Rev. Mar. Sci. (2023).
192. Oliver, E. C. J. et al. Marine Heatwaves. Annu.Rev. Mar. Sci. 13, 313–342 (2021).
193. Bell, J. J. et al. Marine heat waves drive bleaching and necrosis of temperate sponges. Current Biology 33, 158-163.e2 (2023).
194. Leon, P. et al. Relationship between shell integrity of pelagic gastropods and carbonate chemistry parameters at a Scottish Coastal Observatory monitoring site. ICES Journal of Marine Science 77, 436–450 (2020).
195. Findlay, H. et al. Climate change impacts on ocean acidification relevant to the UK and Ireland. MCCIP Science Review 2 (2022).
196. Wolf, J., Woolf, D. & Bricheno, L. Impacts of climate change on storms and waves relevant to the coastal and marine environment around the UK. MCCIP Science Review 2020, 132–157 (2020).
197. Vanem, E. & Bitner-Gregersen, E. M. Stochastic modelling of long-term trends in the wave climate and its potential impact on ship structural loads. Applied Ocean Research 37, 235–248 (2012).
198. Bitner-Gregersen, E. M., Eide, L. I., Horte, T. & Skjong, R. Potential Impact of Climate Change on Design of Ship and Offshore Structures. in Ship and Offshore Structure Design in Climate Change Perspective 43–52 (Springer Berlin Heidelberg, 2013).
199. Thompson, R. C. et al. Lost at Sea: Where Is All the Plastic? Science 304, 838–838 (2004).
200. Stafford, R. & Jones, P. J. S. Viewpoint – Ocean plastic pollution: A convenient but distracting truth? Marine Policy 103, 187–191 (2019).
201. Ford, H. V. et al. The fundamental links between climate change and marine plastic pollution. Science of The Total Environment 806, 150392 (2022).
202. Bergmann, M. et al. Plastic pollution in the Arctic. Nat Rev Earth Environ 3, 323–337 (2022).
203. Wyllie, J. Oil industry dumping tons of microplastics into North Sea each year. Press and Journal (2018).
204. Knutsen, H. et al. Microplastic accumulation by tube-dwelling, suspension feeding polychaetes from the sediment surface: A case study from the Norwegian Continental Shelf. Marine Environmental Research 161, 105073 (2020).
205. La Beur, L. et al. Baseline Assessment of Marine Litter and Microplastic Ingestion by Cold-Water Coral Reef Benthos at the East Mingulay Marine Protected Area (Sea of the Hebrides, Western Scotland). Frontiers in Marine Science 6, (2019).
206. Wright, S. L., Rowe, D., Thompson, R. C. & Galloway, T. S. Microplastic ingestion decreases energy reserves in marine worms. Current Biology 23, R1031–R1033 (2013).
207. Roman, L., Schuyler, Q., Wilcox, C. & Hardesty, B. D. Plastic pollution is killing marine megafauna, but how do we prioritize policies to reduce mortality? Conservation Letters 14, e12781 (2021).
208. Adyel, T. M. & Macreadie, P. I. Plastics in blue carbon ecosystems: a call for global cooperation on climate change goals. The Lancet Planetary Health 6, e2–e3 (2022).
209. Smith, M., Love, D. C., Rochman, C. M. & Neff, R. A. Microplastics in Seafood and the Implications for Human Health. Current Environmental Health Reports 5, 375–386 (2018).
210. Bauer, F. & Fontenit, G. Plastic dinosaurs – Digging deep into the accelerating carbon lock-in of plastics. Energy Policy 156, 112418 (2021).
211. Carpenter, S. Why The Oil Industry’s $400 Billion Bet On Plastics Could Backfire. Forbes (2020).
212. Lo, J. Plastics resolution tees up battle over oil industry’s plan B, Climate Home News. Climate Home News (2022).
213. Oceana. The Cost of Amazon’s Plastic Denial on the World’s Oceans. (2022).
214. BP. BP Energy Outlook – 2018 edition. (2018).
215. Shell. 4 Segment information - Shell Annual Report 2020. (2021).
216. International Energy Agency. The Future of Petrochemicals, (2018).
217. BEIS. UK Offshore Energy Strategic Environmental Assessment 4 (OESEA4).
218. CIEEM. The Guidelines for Ecological Impact Assessment in the UK and Ireland. (2018).
219. Barker, A. & Jones, C. A critique of the performance of EIA within the offshore oil and gas sector. Environmental Impact Assessment Review 43, 31–39 (2013).
220. Hancox, E. QUALITY REVIEW OF OFFSHORE PETROLEUM DEVELOPMENT ENVIRONMENTAL STATEMENTS AGAINST THE EIA DIRECTIVE. 50 (2019).
221. Clark, M. R., Durden, J. M. & Christiansen, S. Environmental Impact Assessments for deep-sea mining: Can we improve their future effectiveness? Marine Policy 114, (2020).
222. OSPAR. Status Assessment 2022 - Deep-sea sponge aggregations. (2022).
223. OPRED. Environmental Statement Summary - Alligin Development.(2018).
224. BP. BP announces first oil from Alligin field, west of Shetland | News and insights | Home.
225. BEIS & OPRED. Offshore Energy Strategic Environmental Assessment (SEA): An overview of the SEA process. (2023).
226. Currie, D. R. & Isaacs, L. R. Impact of exploratory offshore drilling on benthic communities in the Minerva gas field, Port Campbell, Australia. Marine Environmental Research 59, 217–233 (2004).
227. Ellis, J., Fraser, G. & J, R. Discharged drilling waste from oil and gas platforms and its effects on benthic communities. Marine Ecology Progress Series 456, 285–302 (2012).
228. Gates, A. R. & Jones, D. O. B. Recovery of Benthic Megafauna from Anthropogenic Disturbance at a Hydrocarbon Drilling Well (380 m Depth in the Norwegian Sea). PLOS ONE 7, e44114 (2012).
229. Stein J E, Reichert W L, & Varanasi U. Molecular epizootiology: assessment of exposure to genotoxic compounds in teleosts. Environmental Health Perspectives 102, 19–23 (1994).
230. Gerrard, S., Grant, A., Marsh, R. & London, C. Drill cuttings piles in the North Sea: management options during platform decommissioning. Centre for Environmental Risk, Res. Rpt (1999).
231. Helm, R. C. et al. Overview of effects of oil spills on marine mammals. Handbook of oil spill science and technology 455–475 (2014).
232. Venn-Watson, S. et al. Adrenal Gland and Lung Lesions in Gulf of Mexico Common Bottlenose Dolphins (Tursiops truncatus) Found Dead following the Deepwater Horizon Oil Spill. PLOS ONE 10, e0126538 (2015). 233. OSPAR. Precautionary Principle. (2022).
234. Beyond Oil and Gas Alliance (2022). (2022).
235. Linde, L., Sanchez, F., Mete, G. & Lindberg, A. North Sea oil and gas transition from a regional and global perspective. (2022).
236. NSW Government. NSW Government rules out commercial offshore exploration and mining. (2022).
237. Government of Canada. Protection Standardsto better conserve our oceans. (2022).
238. Kapoor, A., Fraser, G. S. & Carter, A. Marine conservation versus offshore oil and gas extraction: Reconciling an intensifying dilemma in Atlantic Canada. The Extractive Industries and Society 8, 100978 (2021).
239. Fisheries and Oceans Canada. Backgrounder: Laurentian Channel Marine Protected Area. (2019).
240. Office of National Marine Sanctuaries. Regulations. (No date).
241. Papahānaumokuākea Marine National Monument. Papahānaumokuākea Marine National Monument Permitting. (No date).
242. Great Barrier Reef Marine Park Authority. Activities and use. (2022).
243. Jaspars, M. et al. The marine biodiscovery pipeline and ocean medicines of tomorrow. Journal of the Marine Biological Association of the United Kingdom 96, 151–158 (2016).
244. Hyder, K., Maravelias, C. D., Kraan, M., Radford, Z. & Prellezo, R. Marine recreational fisheries — current state and future opportunities. ICES Journal of Marine Science 77, 2171–2180 (2020).
245. White, M. P., Elliott, L. R., Gascon, M., Roberts, B. & Fleming, L. E. Blue space, health and well-being: A narrative overview and synthesis of potential benefits. Environmental Research 191, 110169 (2020).
246. Venegas-Li, R. et al. Global assessment of marine biodiversity potentially threatened by offshore hydrocarbon activities. Global Change Biology 25, 2009–2020 (2019).
247. Gattuso, J.-P. et al. Ocean solutions to address climate change and its effects on marine ecosystems. Frontiers in Marine Science 337 (2018).
248. IAMMWG, C. C. & Siemensma, M. A Conservation Literature Review for the Harbour Porpoise (Phocoena phocoena). JNCC Report (2015).
249. Evans, P. & Waggitt, J. Impacts of climate change on Marine Mammals, relevant to the coastal and marine environment around the UK. (2020).
250. HELCOM. Red List of Baltic Sea underwater biotopes, habitats and biotope complexes. (2013).
251. Borrell, A. PCB and DDT in blubber of cetaceans from the northeastern north Atlantic. Marine Pollution Bulletin 26, 146–151 (1993).
252. Law, R. J. & Whinnett, J. A. Polycyclic aromatic hydrocarbons in muscle tissue of harbour porpoises (Phocoena phocoena) from UK waters. Marine Pollution Bulletin 24, 550–553 (1992).
253. Heuvel-Greve, M. J. van den et al. Polluted porpoises: Generational transfer of organic contaminants in harbour porpoises from the southern North Sea. Science of The Total Environment 796, 148936 (2021).
254. Graham, I. M. et al. Harbour porpoise responses to pile-driving diminish over time. Royal Society Open Science 6, 190335 (2019).
255. Todd, V. L., Williamson, L. D., Couto, A. S., Todd, I. B. & Clapham, P. J. Effect of a new offshore gas platform on harbor porpoises in the Dogger Bank. Marine Mammal Science 38, 1609–1622 (2022).
256. Jarvela Rosenberger, A. L., MacDuffee, M., Rosenberger, A. G. J. & Ross, P. S. Oil Spills and Marine Mammals in British Columbia, Canada: Development and Application of a Risk-Based Conceptual Framework. Archives of Environmental Contamination and Toxicology 73, 131–153 (2017).
257. Helm, R. C. et al. Overview of Effects of Oil Spills on Marine Mammals. in Handbook of Oil Spill Science and Technology 455–475 (2014).
258. Williams, R. et al. Levels of polychlorinated biphenyls are still associated with toxic effects in harbor porpoises (Phocoena phocoena) despite having fallen below proposed toxicity thresholds. Environmental Science & Technology 54, 2277–2286 (2020).
259. Santos, M. & Pierce, G. The diet of harbour porpoise (Phocoena phocoena) in the Northeast Atlantic. Oceanogr Mar Biol Annu Rev 41, 355–390 (2003).
260. Hogg, M. et al. Deep-sea sponge grounds: reservoirs of biodiversity. UNEP-WCMC biodiversity series 32, 1–86 (2010).
261. Lea-Anne Henry & Roberts, J. Applying the OSPAR habitat definitions of deep-sea sponge aggregations to verify suspected records of the habitat in UK waters. 508 (2014).
262. Cathalot, C. et al. Cold-water coral reefs and adjacent sponge grounds: hotspots of benthic respiration and organic carbon cycling in the deep sea. Frontiers in Marine Science 2, (2015).
263. JNCC. North-east Faroe-Shetland Channel MPA: Supplementary Advice on the Conservation Objectives (SACO). (2018).
264. Howell, K., Davies, J. & Narayanaswamy, B. Identifying deep sea megafaunal epibenthic assemblages for use in habitat mapping and marine protected area network design. Journal of the Marine Biological Association of the United Kingdom 90, 33–68 (2010).
265. ICES. A suggestive list of deep-water VMEs and their characteristic taxa. https://www.ices.dk/data/Documents/VME/VMEs%20and%20 their%20taxa.pdf (2020).
266. ICES. ICES/NAFO JOINT WORKING GROUP ON DEEP-WATER ECOLOGY (WGDEC). file:///C:/ Users/owner/Downloads ICESNAFOJointWorkingGrouponDeepwaterEcologyWGDEC_Republished.pdf (2020).
267. Indraningrat, A. A. G., Smidt, H. & Sipkema, D. Bioprospecting Sponge-Associated Microbes for Antimicrobial Compounds. Marine Drugs 14, (2016).
268. Cooley, S. et al. Oceans and coastal ecosystems and their services In: in Climate Change 2022: Impacts, adaptation and vulnerability. Contribution of the WGII to the 6th assessment report of the intergovernmental panel on climate change IPCC AR6 WGII (Cambridge University Press, 2022).
269. Daniel O. B. Jones, Ian R. Hudson, & Brian J. Bett. Effects of physical disturbance on the cold-water megafaunal communities of the Faroe–Shetland Channel. Mar Ecol Prog Ser 319, 43–54 (2006).
270. Tjensvoll I, Kutti T, Fosså JH, & Bannister RJ. Rapid respiratory responses of the deep-water sponge Geodia barretti exposed to suspended sediments. Aquat Biol 19, 65–73 (2013).
271. Henry, L.-A., Harries, D., Kingston, P. & Roberts, J. M. Historic scale and persistence of drill cuttings impacts on North Sea benthos. Marine Environmental Research 129, 219–228 (2017).
272. BBC News. Cambo oil field project ‘could jeopardise deep sea life’. BBC News (2021).
273. SICCAR POINT ENERGY. 2021. Cambo Oil Field, UKCS Blocks 204/4a, 204/5a, 204/9a and 204/10a Environmental Impact Assessment (EIA). https://assets.publishing.service.gov.uk/ government/uploads/system/uploads/attachment_data/file/991817/D-4261-2021_-_ES.pdf (2021).
274. Webster, L. et al. Monitoring of Polycyclic Aromatic Hydrocarbons (PAHs) in Scottish Deepwater environments. Marine Pollution Bulletin 128, 456–459 (2018).
275. Luter, H. M. et al. The Effects of Crude Oil and Dispersant on the Larval Sponge Holobiont. mSystems 4, e00743-19 (2019).
276. Kahn, A. S., Yahel, G., Chu, J. W. F., Tunnicliffe, V. & Leys, S. P. Benthic grazing and carbon sequestration by deep-water glass sponge reefs. Limnology and Oceanography 60, 78–88 (2015).
277. Guihen, D., White, M. & Lundälv, T. Temperature shocks and ecological implications at a cold-water coral reef. Marine Biodiversity Records 5, (2012).
278. OSPAR Commission. Background Document for Ocean quahog Arctica islandica. https:// qsr2010.ospar.org/media/assessments/Species/ P00407_Ocean_quahog.pdf (2010).
279. JNCC and Natural England. Review of the MCZ Features of Conservation Importance. https://data.jncc.gov.uk/data/94f961af-0bfc4787-92d7-0c3bcf0fd083/MCZ-review-foci201605-v7.0.pdf (2016).
280. Garcia, S. et al. Protecting the North Sea: Holderness. 32 (2019).
281. Department of Agriculture, Environment and Rural Affairs. Conservation Objectives and Potential Management Options: Outer Belfast Lough Marine Conservation Zone (MCZ). https://niopa. qub.ac.uk/bitstream/NIOPA/5164/1/Conservation%20Objectives%20and%20Potential%20 Management%20Options%20-%20Outer%20 Belfast%20Lough%20MCZ_0.pdf (2016).
282. Hawes, J., Noble-James, T., Lozach, S., Archer-Rand, S., & Cunha, A. North East of Farnes Deep Marine Conservation Zone (MCZ) Monitoring Report 2016.
283. Mazik, K, S. N. et al. A review of the recovery potential and influencing factors of relevance to the management of habitats and species within Marine Protected Areas around Scotland. (2015).
284. Offshore Petroleum Regulator for Environment and Decommissioning. Talbot Field Development. https://www.gov.uk/government/ publications/talbot-field-development (2022).
285. Steimle, F.W., Boehm, P.D., Zdanowicz, V.S., & Bruno, R.A. Organic and trace metal levels in ocean quahog, Arctica islandica Linne, from the Northwestern Atlantic. FISHERY BULLETIN 84, (1986).
286. Tyler-Walters, H. & Hiscock, K. Arctica islandica Icelandic cyprine. In Tyler-Walters H. and Hiscock K. (eds) Marine Life Information Network: Biology and Sensitivity Key Information Reviews. Plymouth: Marine Biological Association of the United Kingdom. in (2017).
287. Ridgway, I. D. & Richardson, C. A. Arctica islandica: the longest lived non colonial animal known to science. Reviews in Fish Biology and Fisheries 21, 297–310 (2011).
288. Butler, P. G., Wanamaker, A. D., Scourse, J. D., Richardson, C. A. & Reynolds, D. J. Variability of marine climate on the North Icelandic Shelf in a 1357-year proxy archive based on growth increments in the bivalve Arctica islandica. Palaeogeography, Palaeoclimatology, Palaeoecology 373, 141–151 (2013).
289. Estrella-Martínez, J. et al. Reconstruction of Atlantic herring ( Clupea harengus ) recruitment in the North Sea for the past 455 years based on the δ 13 C from annual shell increments of the ocean quahog ( Arctica islandica ). Fish and Fisheries 20, (2019).
290. Butler, P. G. et al. Is there a reliable taphonomic clock in the temperate North Atlantic? An example from a North Sea population of the mollusc Arctica islandica. Palaeogeography, Palaeoclimatology, Palaeoecology 560, 109975 (2020).
291. Arellano-Nava, B. et al. Destabilisation of the Subpolar North Atlantic prior to the Little Ice Age. Nature Communications 13, 5008 (2022).
292. Stott, K. et al. The potential of Arctica islandica growth records to reconstruct coastal climate in north west Scotland, UK. Quaternary Science Reviews 29, 1602–1613 (2010).
293. Liehr, G. A., Zettler, M. L., Leipe, T. & Witt, G. The ocean quahog Arctica islandica L.: a bioindicator for contaminated sediments. Marine Biology 147, 671–679 (2005).
294. OSPAR Commission. List of Threatened and/or Declining Species & Habitats. OSPAR Commission https://www.ospar.org/work-areas/ bdc/species-habitats/list-of-threatened-declining-species-habitats (2008).
295. Witbaard, R. & Bergman, M. J. N. The distribution and population structure of the bivalve Arctica islandica L. in the North Sea: what possible factors are involved? Journal of Sea Research 50, 11–25 (2003).
296. Ballesta-Artero, I., Janssen, R., Meer, J. van der & Witbaard, R. Interactive effects of temperature and food availability on the growth of Arctica islandica (Bivalvia) juveniles. Marine Environmental Research 133, 67–77 (2018).
297. Brey, T., Arntz, W. E., Pauly, D. & Rumohr, H. Arctica (Cyprina) islandica in Kiel Bay (Western Baltic): growth, production and ecological significance. Journal of Experimental Marine Biology and Ecology 136, 217–235 (1990).
298. JNCC. Faroe-Shetland Sponge Belt Nature Conservation Marine Protected Area: Data Confidence Assessment. https://data.jncc. gov.uk/data/411ea794-b135-4877-9fc8-e3e6c054eef9/FSSB-2-DataConfidenceAssessment-v5.0.pdf (2014).
299. Hopkins, C. R., Bailey, D. M. & Potts, T. Scotland’s Marine Protected Area network: Reviewing progress towards achieving commitments for marine conservation. Marine Policy 71, 44–53 (2016).
300. Solandt, J.-L., Pikesley, S. K., Trundle, C. & Witt, M. J. Revisiting UK Marine Protected Areas governance: A case study of a collaborative approach to managing an English MPA. Aquatic Conservation: Marine and Freshwater Ecosystems 30, 1829–1835 (2020).
301. Kröncke, I. & Knust, R. The Dogger Bank: A special ecological region in the central North Sea. Helgoländer Meeresuntersuchungen 49, 335–353 (1995).
302. Plumeridge, A. A. & Roberts, C. M. Conservation targets in marine protected area management suffer from shifting baseline syndrome: A case study on the Dogger Bank. Marine Pollution Bulletin 116, 395–404 (2017).
303. JNCC. Southern North Sea MPA – Relevant Documentation & Conservation Advice 2019. https://hub.jncc.gov.uk/assets/206f2222-5c2 b-4312-99ba-d59dfd1dec1d#SouthernNorthSea-conservation-advice.pdf (2019).
304. JNCC. Progress towards completion of the UK network of marine Special Areas of Conservation for Annex I qualifying features. https://hub. jncc.gov.uk/assets/ab711067-5fc2-43f4-b690- 4d6f277d5346 (2013).
305. Jak, R.G., Bos, O.G., Witbaard, R, & Lindeboom, H.J. Conservation objectives for Natura 2000 sites (SACs and SPAs) in the Dutch sector of the North Sea. (2009).
306. Eggleton, J. et al. Dogger Bank SCI 2014 Monitoring R&D Survey Report. (2017).
307. Diesing, M. et al. Understanding the marine environment: seabed habitat investigations of the Dogger Bank offshore draft SAC. (2009).
308. Jones EL et al. Patterns of space use in sympatric marine colonial predators reveal scales of spatial partitioning. Mar Ecol Prog Ser 534, 235–249 (2015).
309. Cucknell, A.-C., Boisseau, O., Leaper, R., McLanaghan, R. & Moscrop, A. Harbour porpoise (Phocoena phocoena) presence, abundance and distribution over the Dogger Bank, North Sea, in winter. Journal of the Marine Biological Association of the United Kingdom 97, 1455–1465 (2017).
310. Reid, J. B., Evans, P. G. & Northridge, S. P. Atlas of cetacean distribution in north-west European waters. (Joint Nature Conservation Committee, 2003).
311. JNCC. Supplementary Advice on Conservation Objectives for Dogger Bank Special Area of Conservation. https://data.jncc.gov.uk/ data/1422e961-edfb-40e8-b1ad-2eaf67cf21f0/ FSSB-3-SACO-V1.0.pdf (2018).
312. Erbe, C. et al. The Effects of Ship Noise on Marine Mammals—A Review. Frontiers in Marine Science 6, (2019).
313. JNCC. Supplementary Advice on Conservation Objectives for East of Gannet and Montrose Fields Nature Conservation MPA [Online]. https:// data.jncc.gov.uk/data/7d1e751a-e082-405baad9-51eeaf53dd67/EGM-3-SACO-v1.0.pdf (2018).
314. JNCC. East of Gannet and Montrose Fields MPA. https://jncc.gov.uk/our-work/east-of-gannet-and-montrose-fields-mpa/#conservation-advice (2021).
315. North Sea Transition Authority (NSTA). NSTA. 33rd Petroleum Licensing Round, Southern North Sea: SNS Cluster Rationale [Online]. https://www.nstauthority.co.uk/media/8425/ sns-cluster-rationale-accessible-7-october.pdf (2022).
316. JNCC. Management Options Paper: EAST OF GANNET AND MONTROSE FIELDS NATURE CONSERVATION MARINE PROTECTED AREA (MPA). https://data.jncc.gov.uk/data/18a1c6a2- 7dc3-4ee5-b6fd-09f756d2d30c/EGM-4-ManagementOptionsPaper-v4.0.pdf (2014).
317. JNCC. East of Gannet and Montrose Fields Nature Conservation MPA: Data Confidence Assessment. https://data.jncc.gov.uk/data/18a1c6a2-7dc3-4ee5-b6fd-09f756d2d30c/ EGM-2-DataConfidenceAssessment-v5.0.pdf (2014).
318. McCabe, C., McBreen, F., & O’Connor, J. East of Gannet and Montrose Fields MPA Monitoring Report 2015 (Version 2). https://data. jncc.gov.uk/data/78cb6096-16a3-4904-9014- f17fc56d402a/JNCC-MSS-Report-1-Version2- WEB.pdf.
319. OSPAR. Background Document for Seapen IN DEEP WATER IN DEEP WATER 45 and Burrowing megafauna communities. https:// www.ospar.org/documents?v=7261 (2010).
320. JNCC. UK Biodiversity Action Plan Priority Habitat Descriptions Mud Habitats in Deep Water. https://data.jncc.gov.uk/data/c9721550-e422- 4181-805d-2a0b58afa9d7/UKBAP-BAPHabitats-37-MudHabitatsDeepWater.pdf (2008).
321. Sabatini, M. & Hill, J.M. Sabatini, M. & Hill, J.M. 2008. Nephrops norvegicus Norway lobster. https://dx.doi.org/10.17031/marlinsp.1672.1 (2008).
322. Hibiscus Petroluem. Teal West Development: Environmental Statement. https://assets. publishing.service.gov.uk/government/uploads/ system/uploads/attachment_data/file/1099286/ Teal_West_Environmental_Statement_1_Redacted.pdf (2022).
323. Reid, J. B., Evans, P. G. & Northridge, S. P. Atlas of cetacean distribution in north-west European waters. (Joint Nature Conservation Committee, 2003).
324. DECC. Environmental Statement (ES) Summary and Sign-Off Godwin Development. https:// assets.publishing.service.gov.uk/government/ uploads/system/uploads/attachment_data/ file/599631/TalismanGodwin.pdf (2011).
325. Maldonado, Manuel et al. Sponge Grounds as Key Marine Habitats: A Synthetic Review of Types, Structure, Functional Roles, and Conservation Concerns. in Marine Animal Forests: The Ecology of Benthic Biodiversity Hotspots 145–183 (Springer International Publishing, 2017).
326. Turrell, W. R., Slesser, G., Adams, R. D., Payne, R. & Gillibrand, P. A. Decadal variability in the composition of Faroe Shetland Channel bottom water. Deep Sea Research Part I: Oceanographic Research Papers 46, 1–25 (1999).
327. Bett, B. J. UK Atlantic Margin Environmental Survey: Introduction and overview of bathyal benthic ecology. Continental Shelf Research 21, 917–956 (2001).
328. Tangye, Tom. What else is lurking in the depths of the Faroe-Shetland Sponge Belt MPA? JNCC Blog https://jncc.gov.uk/about-jncc/jnccblog/archive/what-else-is-lurking-in-the-depthsof-the-faroe-shetland-sponge-belt-mpa/ (2021).
329. Hastie, G. D., Swift, R. J., Slesser, G. & Turrell, W. R. Sperm whale distribution and seasonal density in the Faroe Shetland Channel. in (2003).
330. Weir, C. R., Pollock, C., Cronin, C. & Taylor, S. Cetaceans of the Atlantic Frontier, north and west of Scotland. Continental Shelf Research 21, 1047–1071 (2001).
331. Macleod, K., Simmonds, M. & Murray, E. Summer distribution and relative abundance of cetacean populations off north-west Scotland. Journal of the Marine Biological Association of the UK 83, 1187–1192 (2003).
332. Vad, J. et al. Environmental controls and anthropogenic impacts on deep-sea sponge grounds in the Faroe-Shetland Channel, NE Atlantic: the importance of considering spatial scale to distinguish drivers of change. ICES Journal of Marine Science 77, 451–461 (2020).